Cancer du sein : une simple prise de sang pourrait bientôt détecter la maladie très tôt

De nouvelles technologies combinant lasers, intelligence artificielle et génomique pourraient permettre d’identifier un cancer du sein avant même l’apparition des premiers symptômes, grâce à une simple prise de sang.
Un cancer du sein qui n’a encore provoqué aucun symptôme, qui n’est pas visible à la mammographie et dont la patiente ignore encore l’existence… mais déjà détectable grâce à une simple prise de sang. Cela semble presque impossible, et pourtant plusieurs laboratoires travaillent actuellement pour faire de cette possibilité une réalité dans un futur proche.
En Suisse, environ 6800 nouveaux cas de cancer du sein sont diagnostiqués chaque année. Il s’agit du cancer le plus fréquent chez les femmes — plus de 30 % des cancers féminins concernent le sein. La bonne nouvelle, c’est qu’aujourd’hui, 87 % des patientes guérissent. Mais un élément fait toute la différence : le moment du diagnostic. Lorsque la tumeur mesure moins d’un centimètre et n’a pas encore provoqué de symptômes, le taux de survie approche les 98 %. En revanche, lorsque le cancer est découvert à un stade avancé, les probabilités changent considérablement.
Cancer du sein : pourquoi la prévention reste essentielle
Force, renaissance et actions conscientes : l’IA devient précieuse pour le dépistage mammographique.
Le diagnostic précoce, clé du traitement du cancer du sein
Aujourd’hui, la mammographie reste le principal outil de dépistage, mais elle présente certaines limites. Elle n’est pas aussi efficace sur tous les types de tissus : environ 40 % des femmes ont une poitrine dense, dans laquelle le tissu glandulaire rend les anomalies plus difficiles à distinguer. Elle n’est pas non plus adaptée aux femmes jeunes et ne peut pas être répétée trop fréquemment en raison de l’exposition aux radiations.
D’où la nécessité de développer des méthodes de diagnostic plus accessibles, répétables et moins invasives, comme une simple prise de sang.
Cette piste de recherche repose sur un constat : dès ses premiers stades, la tumeur interagit avec l’organisme qui l’héberge et laisse derrière elle des traces presque invisibles — fragments d’ADN présentant des altérations caractéristiques, petites molécules d’ARN ou encore modifications de la composition chimique du plasma. Repérer ces indices est possible, mais extrêmement complexe : il faut pour cela des outils de très haute précision.
Étude particulièrement prometteuse
Une équipe de l’Université d’Édimbourg dirigée par le docteur Andy Downes a publié les résultats d’une étude pilote particulièrement prometteuse. La méthode combine la spectroscopie Raman — une technique utilisant un laser — à des algorithmes de machine learning.
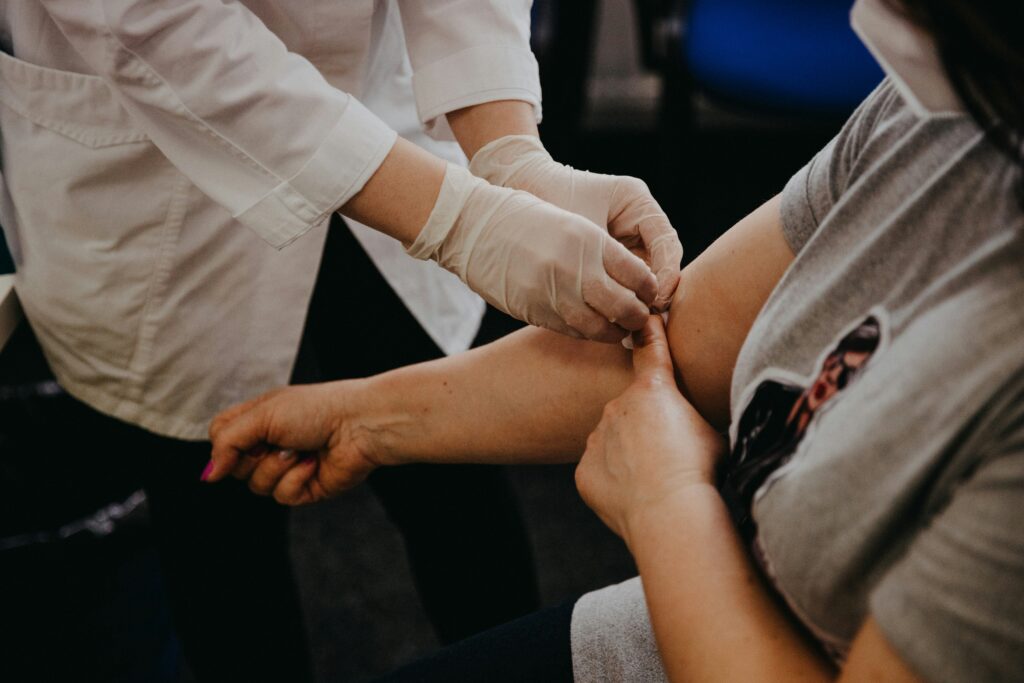
Entraîné sur des échantillons connus, l’algorithme apprend à distinguer les signatures d’un sang sain de celles d’un organisme touché par un cancer, en interprétant l’ensemble des variations comme un véritable langage. Pour la première fois, il a réussi à identifier un cancer du sein de stade 1 directement à partir d’un échantillon sanguin.
Le stade 1 correspond déjà à une tumeur invasive, mais encore extrêmement petite : moins de deux centimètres et sans atteinte des ganglions lymphatiques. Le cancer est donc déjà formé, mais détecté très précocement.
Comment savoir si une chimiothérapie, une radiothérapie ou une chirurgie sont vraiment nécessaires ?
Une autre recherche, menée par l’Université du Michigan et l’Université du Kansas, part d’un diagnostic déjà établi de carcinome canalaire in situ (DCIS), c’est-à-dire un cancer à un stade très précoce, et pose une question essentielle : comment savoir si une patiente a réellement besoin d’une chimiothérapie, d’une radiothérapie ou d’une opération chirurgicale ?
Il s’agit de l’un des diagnostics les plus délicats de l’oncologie moderne. Les cellules anormales restent confinées dans les canaux mammaires et n’ont pas encore envahi les tissus environnants. Autrement dit, il ne s’agit pas encore d’un cancer invasif — et il n’est pas certain qu’il le devienne un jour.
Le problème est qu’il n’existe aujourd’hui aucun système fiable permettant de déterminer quels DCIS évolueront vers un cancer invasif et lesquels resteront stables. Par précaution, toutes les patientes sont donc traitées, ce qui conduit de nombreuses femmes à subir des traitements agressifs et leurs effets secondaires potentiellement inutiles.
Au cœur de cette étude se trouve une technologie de microfluidique baptisée Labyrinth Chip. Le sang analysé circule dans un réseau de microcanaux où les cellules tumorales — plus grandes et plus rigides que les cellules saines — sont séparées physiquement du reste de l’échantillon.
Ces cellules isolées sont ensuite soumises à une analyse génétique afin d’identifier des signaux d’agressivité, de résistance à la chimiothérapie ou encore de capacité à échapper au système immunitaire. L’objectif du test est de déterminer si une patiente doit suivre un traitement standard ou si elle pourrait s’en passer.
Détecter le cancer grâce à l’ADN
Le test Galleri, développé par la société américaine GRAIL, représente aujourd’hui l’approche la plus ambitieuse — et la plus débattue — dans ce domaine.
Il analyse la méthylation de l’ADN circulant dans le sang, c’est-à-dire des modifications chimiques de l’ADN tumoral permettant d’identifier le tissu d’origine du cancer, et promet de détecter les signaux de plus de 50 types de cancers à partir d’une seule prise de sang.
Cette technologie est bien réelle, fondée sur des bases biologiques solides et testée dans la plus vaste étude clinique jamais menée sur un test de ce type.
Mais le test reste encore imparfait. Il améliore les diagnostics, sans être suffisamment performant pour justifier, à ce stade, un déploiement massif. Concernant le cancer du sein en particulier, l’analyse du cfDNA se heurte à une limite biologique fondamentale : à un stade précoce, les tumeurs mammaires libèrent des quantités extrêmement faibles d’ADN dans le sang, rendant le signal très difficile à détecter.
C’est là tout le paradoxe technologique : plus le diagnostic est précoce — et donc précieux —, plus les outils peinent à identifier les signaux.
Les tests de biopsie liquide déjà disponibles
Au-delà des études encore en cours de validation, une biopsie liquide est déjà utilisée en pratique clinique : l’analyse de l’ADN tumoral circulant (ctDNA).
Elle sert à surveiller la réponse à un traitement, détecter les récidives plusieurs mois avant les techniques d’imagerie traditionnelles et établir le profil moléculaire d’un cancer métastatique afin de choisir la thérapie la plus efficace.
Cette biopsie liquide déjà disponible représente un véritable outil de médecine de précision, capable de transformer les traitements — et parfois le destin — des patientes.
Perfectionner les outils diagnostiques est un processus long, mais la trajectoire est désormais clairement engagée. Les chercheurs apprennent progressivement à lire avec toujours plus de précision — et à des stades toujours plus précoces — les traces laissées par les tumeurs dans le sang.
Autrice : Claudia Loiacono
Cet article a été traduit en français et adapté pour la Suisse après avoir initialement été publié sur elle.com/it. Retrouvez tous les autres articles de cette édition sur le site web officiel.